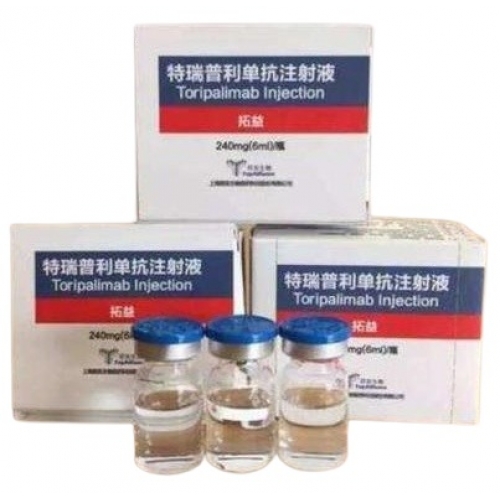
特瑞普利单抗在国内上市了吗

特瑞普利单抗在国内上市了吗,特瑞普利单抗(Toripalimab)于2018年12月17日中国批准上市,于2023年底获得美国FDA批准上市。
特瑞普利单抗(Toripalimab)是一种新型的免疫治疗药物,主要用于治疗多种癌症,包括尿路上皮癌、鼻咽癌和黑色素瘤等。近年来,随着国内对创新药物的重视及批准流程的加快,这款药物的上市状况备受关注。本文将围绕特瑞普利单抗在国内的上市情况进行探讨。
1. 特瑞普利单抗的药物背景
特瑞普利单抗是一种针对程序性死亡-1(PD-1)蛋白的单克隆抗体,通过增强免疫系统对肿瘤细胞的攻击能力来发挥抗癌作用。该药物的研发团队致力于为中国患者提供更多可选的免疫治疗方案,尤其是在传统治疗无效或复发的情况下。
2. 国内上市进程
在中国,特瑞普利单抗的临床试验数据表明其在治疗尿路上皮癌、鼻咽癌和黑色素瘤中具有良好的疗效和安全性。随着临床试验的成功,特瑞普利单抗的上市申请于2020年获得了国家药品监督管理局(NMPA)的批准,成为国内首个获得上市许可的PD-1免疫检查点抑制剂之一。
3. 临床应用与市场反馈
特瑞普利单抗自上市以来,已在多个医疗机构中开展了广泛的临床应用。根据患者反馈,该药物在提高生存率及改善生活质量方面的表现都得到了肯定。同时,医疗界对于免疫治疗的普及也促使更多医生了解并使用该药,减少了患者的治疗负担。
4. 前景与挑战
尽管特瑞普利单抗在国内上市并取得了一定的成功,但未来的发展仍面临挑战。例如,如何提高药物的经济可及性,以及在多种癌症类型中的推广应用,都是需要继续努力的方向。随着更多临床数据的积累和研究的深入,特瑞普利单抗未来有望在更多领域发挥重要作用。
特瑞普利单抗在国内的上市标志着中国在免疫疗法领域的重要进展,为癌症患者带来了新的希望与选择。随着科学技术的不断进步和临床研究的开展,未来我们期待看到更多创新药物加入治疗阵营,进一步改善癌症患者的生存质量。