IDO1抑制剂的再利用:治疗阿尔兹海默病的新希望
 找药助理
找药助理
关键词: #健康资讯
 找药助理
找药助理
关键词: #健康资讯
近年来,科学家们在寻找治疗神经变性疾病的过程中取得了重大进展,特别是关于阿尔兹海默病这种最常见的痴呆症。传统的治疗方法主要集中于缓解症状和延缓疾病进展,但很少有疗法能够直接阻止或逆转疾病的发生。然而,最新的研究表明,一种目前用于治疗癌症的药物——IDO1抑制剂,或许能够为阿尔兹海默病的治疗提供全新的方向。
阿尔兹海默病与大脑代谢的关联
阿尔兹海默病是一种常见的神经变性疾病,患者的认知功能逐渐衰退,最终丧失基本的生活能力。其典型特征是大脑中的淀粉样蛋白斑块和tau蛋白缠结的形成,这些异常的蛋白质积累会导致神经元的损伤和死亡,进而引发记忆力丧失、认知障碍等症状。根据2023年美国疾病控制与预防中心(CDC)的数据,目前约有670万美国人患有阿尔兹海默病,预计到2060年,这一数字可能会增加至三倍。
过去的研究主要集中在清除大脑中的这些有害蛋白质,但效果有限,因为当患者出现明显症状时,蛋白质的积累已经对大脑造成了不可逆的损害。近期的一项突破性研究表明,阿尔兹海默病不仅仅与蛋白质异常有关,代谢紊乱也是其病理机制中的重要部分。这为研究人员提供了一个新的治疗切入点:通过改善大脑的葡萄糖代谢,或许可以减缓甚至逆转疾病的进展。
IDO1抑制剂的再利用:从癌症到神经变性疾病
由宾夕法尼亚州立大学的科学家们领导的一项研究发现,IDO1抑制剂这一目前用于治疗多种癌症的药物,可能也能用于治疗阿尔兹海默病等神经变性疾病。IDO1(吲哚胺-2,3-双加氧酶)是一种参与机体色氨酸代谢的关键酶,其主要作用是将色氨酸转化为犬尿氨酸,而犬尿氨酸的生成又启动了一系列代谢反应。
在正常情况下,犬尿氨酸途径对于调控机体的免疫反应和提供细胞能量非常重要。然而,当IDO1过度活跃时,它会削弱星形胶质细胞(大脑中的一种支持性细胞)为神经元提供能量的能力。星形胶质细胞主要通过葡萄糖代谢为神经元提供支持,而IDO1的过度活跃会导致这种代谢过程受损,进而影响神经元的功能。研究发现,通过抑制IDO1,星形胶质细胞的葡萄糖代谢得以恢复,从而重新为神经元提供足够的能量支持。
临床前研究的结果
为了验证这一理论,研究团队采用了多种阿尔兹海默病的临床前模型,包括体外细胞实验、体内小鼠实验以及阿尔兹海默病患者的细胞研究。他们发现,阻断IDO1能够显著恢复神经元的代谢功能,并改善实验小鼠的认知表现。更重要的是,这种保护性效应不仅限于一种病理类型。无论是由淀粉样蛋白斑块引起的阿尔兹海默病,还是由tau蛋白缠结引起的神经损伤,IDO1抑制剂都表现出了显著的疗效。
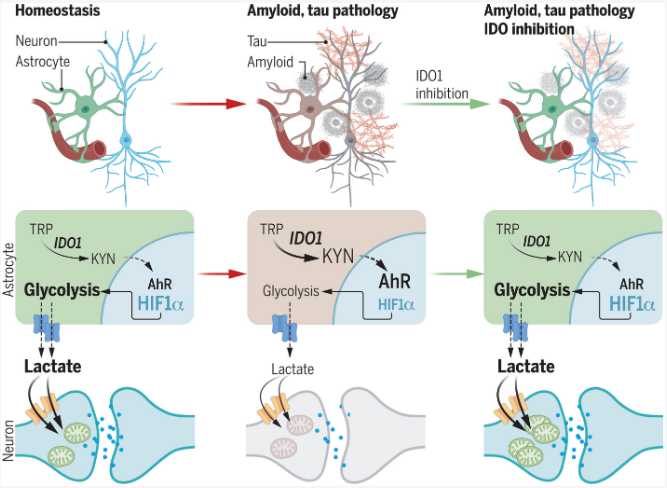
这一发现令人振奋,因为它表明IDO1抑制剂可能跨越多种神经变性疾病的病理机制,而不仅仅局限于一种特定的疾病类型。这为未来的药物开发提供了新的希望,尤其是在治疗阿尔兹海默病的早期阶段,通过改善大脑的代谢环境,或许可以延缓疾病的进展。
更广泛的应用前景:从阿尔兹海默病到其他神经变性疾病
除了阿尔兹海默病之外,研究人员还推测,IDO1抑制剂可能在其他神经变性疾病的治疗中发挥作用。例如,帕金森病和其他与tau蛋白病(如额颞痴呆)相关的疾病也可能受益于这一类药物的治疗。由于这些疾病的发病机制中也存在代谢紊乱和能量供应不足的问题,IDO1抑制剂通过恢复大脑的葡萄糖代谢,可能在广泛的神经变性疾病中发挥治疗作用。
进一步的研究还可以探讨这种药物对正常衰老过程中神经功能下降的影响。随着人类寿命的延长,衰老相关的神经变性问题越来越普遍。如果能够开发出一种药物,在早期阶段阻止或逆转大脑的代谢损伤,将为健康老龄化提供重要的保障。
未来的研究方向与挑战
尽管IDO1抑制剂在临床前研究中表现出显著的潜力,但要将其应用于临床治疗仍面临诸多挑战。首先,需要进行更多的人体临床试验,以验证其在不同神经变性疾病中的疗效和安全性。此外,研究人员还需要确定最佳的用药剂量和时机,确保患者能够在疾病的早期阶段获得最大益处。
另一个重要的研究方向是进一步探讨IDO1抑制剂对其他代谢通路的影响。大脑中的代谢过程极为复杂,IDO1仅仅是其中的一个环节。通过全面了解不同代谢通路之间的相互作用,科学家们可以开发出更为精确的治疗方案,从而为神经变性疾病的治疗带来更大突破。
结语
总之,IDO1抑制剂的发现为阿尔兹海默病等神经变性疾病的治疗带来了全新的希望。通过恢复大脑的葡萄糖代谢,这一类药物有望减缓甚至逆转疾病的进展,尤其是在早期阶段。这不仅为患者带来了福音,也为未来的研究和临床应用提供了宝贵的参考。
随着科学研究的不断深入,我们有理由相信,未来将会有更多基于代谢调控的疗法出现,帮助人们应对包括阿尔兹海默病在内的各种神经变性疾病。通过这一方向的研究,不仅可以改善患者的生活质量,还能为人类健康老龄化的目标提供有力支持。

2025-12-14

2025-12-14

2025-12-14

2025-12-14

2025-12-14