开启非小细胞肺癌靶向治疗新纪元——谷美替尼助力METex14突变患者
 找药助理
找药助理
关键词: #健康资讯
 找药助理
找药助理
关键词: #健康资讯
最近,在山东济南举行了2024年的CSCO指南大会,会议上发布了更新后的《2024年CSCO非小细胞肺癌诊疗指南》,内容有许多重要更新。
该药物是国产原创的一类新药,名为谷美替尼。它已被纳入相关指南,作为治疗METex14外显子跳跃突变(METex14跳变)非小细胞肺癌患者的首选药物。这标志着开启了针对METex14跳变非小细胞肺癌患者的靶向治疗新阶段。
肺癌是我国罹患率和死亡率最高的癌症之一,其中METex14基因突变是导致非小细胞肺癌的重要致癌因素之一。METex14基因突变提示疾病恶化程度更高,预后更差。这部分患者对化疗、免疫疗法,甚至多靶点酪氨酸激酶抑制剂(TKI)的治疗效果都相对有限。以往的临床研究显示,METex14基因突变的非小细胞肺癌患者接受第一线化疗的中位总生存期只有6.7个月。免疫疗法对这类患者也只提升了中位无疾病进展生存期1.9个月。MET-TKI药物如谷美替尼的问世彻底改变了METex14基因突变非小细胞肺癌患者的治疗困境,显著改善了预后。
古美替尼在《2024年CSCO非小细胞肺癌诊疗指南》中被列为一线治疗首选,这是基于GLORY研究结果的优异表现。
GLORY研究是一个非随机、开放标签、跨国多中心的II期研究计划(NCT04270591),旨在纳入已确认患有METex14基因突变的晚期或转移性非小细胞肺癌患者,进行谷美替尼单药疗法。研究的主要目标是由盲审的独立影像评估委员会(BIRC)评估的总体客观缓解率(ORR)。
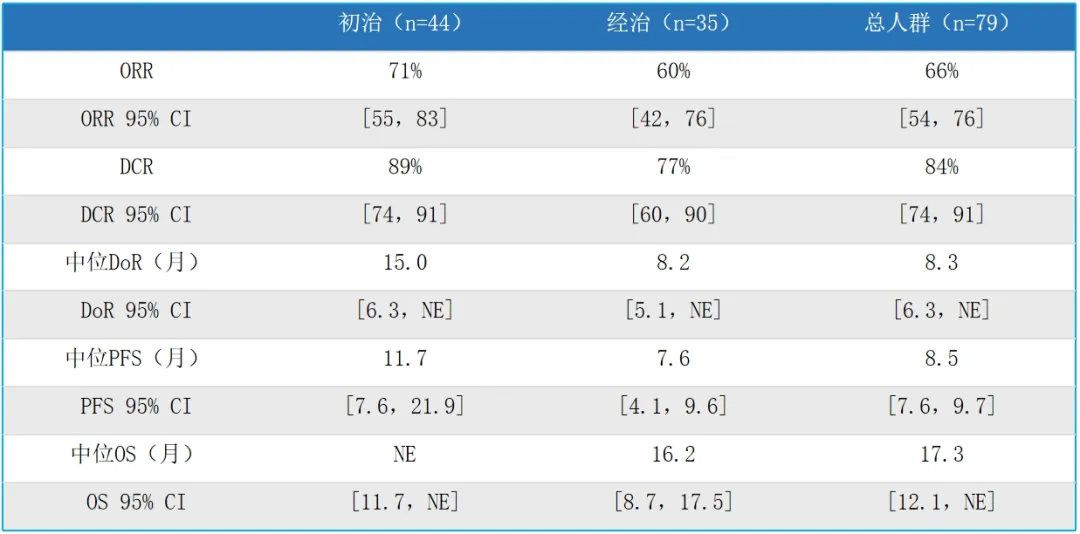
研究总共招募了84位患者,79位患者被纳入有效性分析,其中包括44位初治患者和35位经治患者。中位随访时间为13.5个月。研究结果显示:总体反应率为66%,其中初治患者反应率高达71%,经治患者也达到60%;中位缓解持续时间为8.3个月,初治患者为15.0个月,经治患者为8.2个月;中位无进展生存期为8.5个月,初治患者为11.7个月,经治患者为7.6个月;中位总生存期为17.3个月,初治患者未达到,经治患者为16.2个月。有13位患者有基线脑转移,反应率为85%(11/13),其中5例患者的脑转移被评为靶病灶,在治疗后观察到颅内肿瘤缓解。
谷美替尼在安全性方面表现良好,整体安全性良好,不会出现严重肝毒性、间质性肺病等致命的不良反应,且药物相互作用较少,使用更加安全。
在2024年1月1日开始实施《国家基本医疗保险、工伤保险和生育保险药品目录(2023年版)》时,谷美替尼被确定为唯一医保全线报销的MET-TKI[5]。这明显提升了METex14跳变NSCLC患者获得该药物的便利性,使更多患者能接受精准靶向治疗,既减轻了患者的经济负担,又有助于患者的长期存活和生活质量。
据GLORY研究表明,谷美替尼对中国METex14跳变非小细胞肺癌患者的预后有明显改善,且安全性良好。该疗效和安全性数据来自中国患者,对指导中国临床实践具有重要意义。目前,谷美替尼已列入最新国家医保目录,进一步提高了患者用药的便利性。
顾美替尼被首选推荐并纳入《2024年CSCO非小细胞肺癌诊疗指南》,这标志着METex14突变的NSCLC患者在靶向治疗方面迈出了重要的一步,给患者带来了新的希望!
谷美替尼片是一种口服药物,具有全球独立知识产权,属于强效、高选择性的MET酪氨酸激酶抑制剂(TKI)。该药于2021年9月被中国国家药品监督管理局(NMPA)认定为突破性治疗药物,2022年获得了美国食品药品监督管理局(FDA)颁发的孤儿药资格认定。
2022年12月17日,石药集团与海和药物签署了一份授权协议,协议约定石药集团将负责推动海益坦®(谷美替尼片)在大中华地区(包括香港、澳门、台湾)的商业推广。双方携手合作,共同为更多患者提供健康保障。
2023年3月8日,海益坦®在获得国家药品监督管理局(NMPA)的附加条件批准后上市,可用于治疗患有间质-上皮转化因子(MET)外显子14跳跃突变(METex14跳变)的局部晚期或转移性非小细胞肺癌(NSCLC)的成年患者。

2025-04-13

2025-04-13

2025-04-13

2025-04-13

2025-04-13