MANF过表达在阿尔茨海默病中的作用及其潜在治疗价值
 找药助理
找药助理
关键词: #健康资讯
 找药助理
找药助理
关键词: #健康资讯
中脑星形胶质细胞源性神经营养因子(MANF)是一种非经典神经营养因子,在帕金森病、缺血性卒中及视网膜变性等病理状态中具有神经保护作用。内质网应激可以诱导MANF表达的增加,而在阿尔茨海默病(AD)患者及相关小鼠模型中,也观察到MANF表达的显著上调。然而,MANF上调在AD病理过程中的确切作用尚不明确。
为了揭示MANF在AD中的作用机制,暨南大学粤港澳中枢神经再生研究院杨甦和李晓江团队通过研究不同病理阶段的AD小鼠,深入探讨了MANF与突触功能的分子关系,发现其表达水平的升高与突触病变和认知缺陷密切相关。
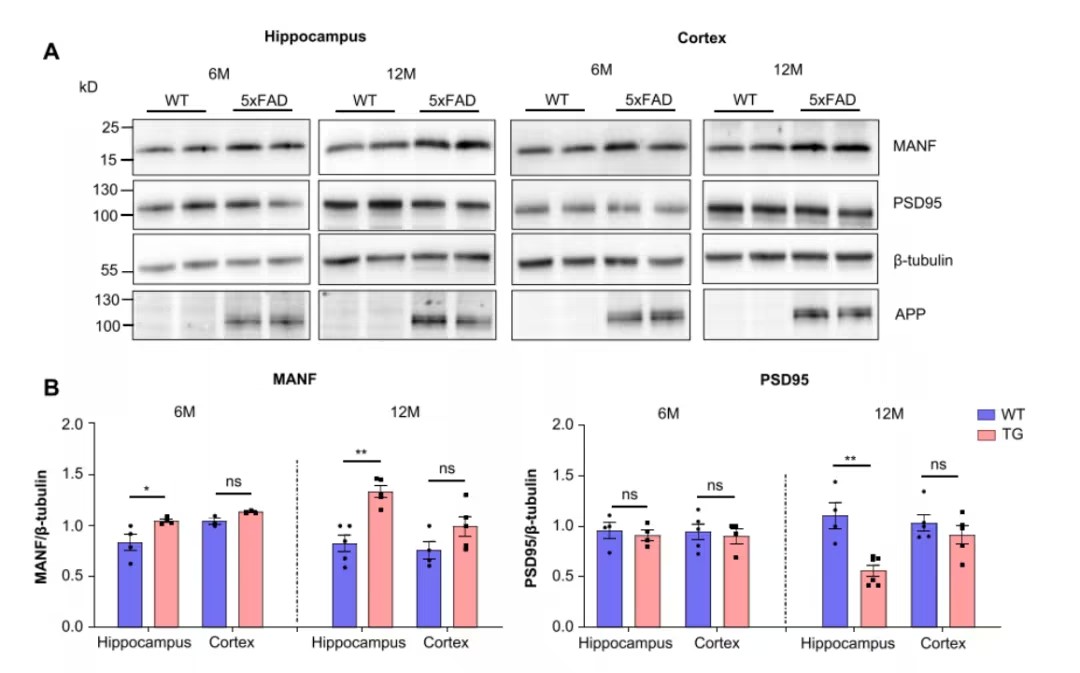
MANF表达与AD小鼠突触病变的关联
研究团队首先分析了不同年龄阶段的AD小鼠模型,发现6月龄小鼠尽管已出现Aβ沉积,星形胶质细胞和小胶质细胞的活化水平升高,但海马突触相关蛋白PSD95的水平并未显著下降,说明此时突触尚未明显丢失。然而,到12月龄时,小鼠的PSD95水平显著降低,同时MANF表达显著增加。免疫荧光检测显示,MANF主要分布在神经元内的内质网中。
在人类AD患者的大脑样本中,也发现了突触丢失与MANF表达上调的相似模式。这提示,MANF可能在突触病变中发挥重要作用。
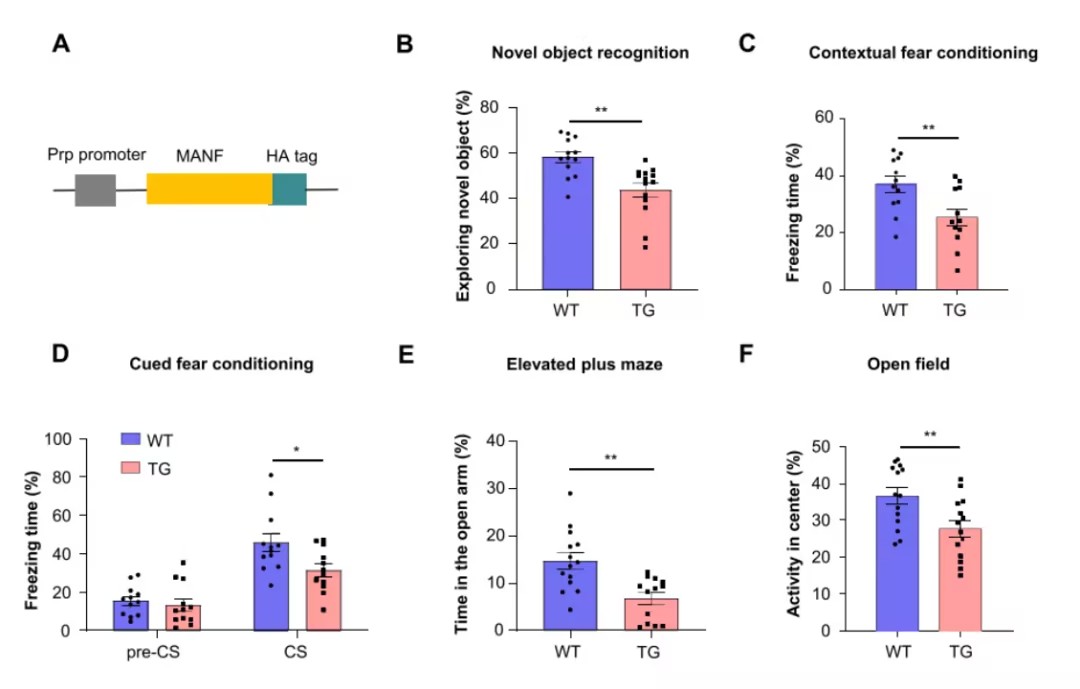
MANF过表达引发认知缺陷与突触丢失
为进一步验证MANF在突触功能中的作用,研究人员构建了MANF过表达的小鼠模型。实验结果表明,与野生型小鼠相比,这些小鼠在6月龄时已经表现出明显的认知障碍和焦虑行为。进一步分析显示,MANF过表达小鼠的海马中突触素和PSD95水平明显降低,突触密度及树突棘数量显著减少。这些现象表明,MANF过表达导致突触结构和功能的显著破坏,可能是认知缺陷的重要原因。
随后,研究人员在小鼠海马区域单独过表达MANF,发现其对突触病变和行为缺陷的影响与全脑MANF过表达的结果相似。这一发现进一步证明,MANF上调对海马突触功能的损害具有局部性作用。
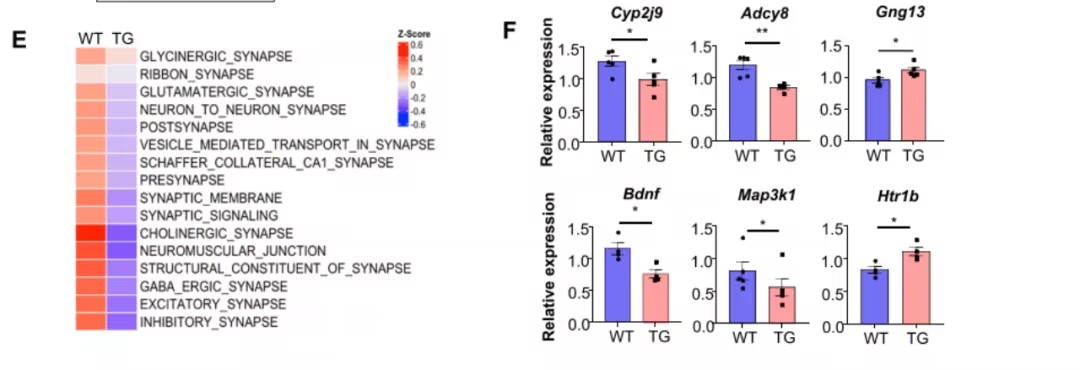
MANF通过影响ELAVL2介导突触基因表达
为了探索MANF调控突触功能的具体机制,研究人员分析了与MANF相互作用的蛋白质,并重点关注ELAV样RNA结合蛋白2(ELAVL2)。ELAVL2是一种调节mRNA稳定性的关键蛋白,已知与突触功能和阿尔茨海默病密切相关。
RNA测序结果表明,MANF过表达小鼠和野生型小鼠之间存在172个差异表达基因,其中许多与突触功能相关基因(如Adcy8、Bdnf等)的转录水平显著降低。这说明,MANF可能通过与ELAVL2相互作用,影响突触相关转录本的稳定性,从而破坏突触功能。
调节MANF表达改善AD小鼠病理表现
研究进一步证实,降低AD小鼠海马中MANF的表达能够显著改善其认知障碍和焦虑行为,同时恢复突触素和PSD95的表达水平。然而,MANF表达的调控并未显著改变Aβ斑块的面积和Aβ42的浓度。这表明,MANF主要通过影响突触结构和功能,而非直接改变Aβ病理,在AD中发挥作用。
结论与启示
综上所述,该研究发现MANF表达的上调与AD海马突触病变及认知功能障碍密切相关,MANF过表达可导致突触密度降低和行为缺陷,而降低MANF水平则能够显著缓解这些病理表现。这为阿尔茨海默病的治疗提供了新的潜在靶点。未来的研究可进一步探索MANF调控的分子机制及其在神经退行性疾病中的治疗潜力。

2025-04-01

2025-04-01

2025-04-01

2025-04-01

2025-04-01