乙肝治疗领域现突破性疗法 企业获突破性认定
 找药助理
找药助理
关键词: #健康资讯
 找药助理
找药助理
关键词: #健康资讯
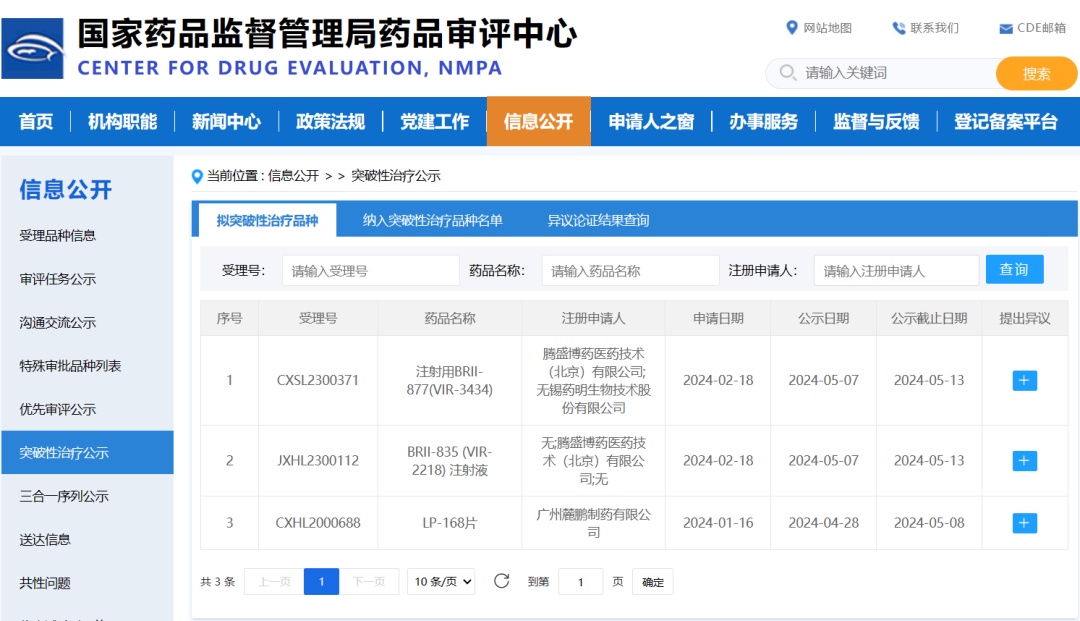
近期,国家明显增加了对创新药的支持,甚至首次在政府工作报告中提及“创新药”,这无疑是对创新药产业莫大的鼓励。最近,根据国家药监局网站公示,腾博药业的两款新型乙肝药物,BRII-835(小RNA干扰物)和BRII-877(乙肝特异性抗体中和物)被认定为具有突破性疗效,有助于加快乙肝治疗疗法的研究进程。自去年11月BRII-179(乙肝治疗疫苗)获突破性认定后,这已经是第二次有两种乙肝药物获此认定。值得一提的是,腾博药业旗下三种乙肝领域的临床研究药物全部获得或拟获得突破性认定,这在国内创新药企业中尚属首次,彰显了其在乙肝治疗领域的卓越全球地位。
经历了这两年资本市场的严冬,腾盛博药的股价已经下跌到历史最低点,今年退出港股通更加雪上加霜。然而,根据公司3月发布的年度报告显示,目前公司拥有20多亿人民币现金,足以支持公司运营至2027年。这一强大的财务支持,再加上三项突破性治疗认证,无疑为公司未来发展打下了坚实基础并提供了竞争优势。
根据最新的年报显示,公司计划在今年进行若干项新的乙肝功能性治愈联合疗法二期研究,同时缩减其他非核心产品线,以寻求外部BD机会。这一资源重新配置使腾盛博药能够全力专注于乙肝功能性治愈领域,表现出对克服乙肝这一严重公共卫生问题的坚定决心。
近年来,治疗乙肝功能性治愈的研究面临许多挑战。腾盛博药与合作伙伴Vir进行了临床试验,积累了大量指导性数据,为研究团队提供了更多科学见解和研究思路。他们提出使用治疗性疫苗BRII-179进行初步筛选和联合治疗,以识别对治疗反应更好的患者,随后为这些患者提供联合疗法,从而提高功能性治愈率。这种研究思路在乙肝研究领域具有独特性。
腾盛博药计划再次获得突破性治疗认定,这将为公司的后期临床试验和注册申报打下坚实基础。考虑到乙肝领域疾病和治疗方案的特殊性,相关临床试验通常需时较长,至少约2年才能初步看到结果。而获得突破性治疗认定有助于企业加快与国家药监局的沟通进程,在后续申报中也能获得优先审评的机会。这一认定不仅是对腾盛博药产品潜力的认可,还是对其过去几年临床试验数据和结果的肯定。
据报道,除了腾盛博药目前正在进行的多个临床项目外,腾盛博药的合作伙伴Vir也将在今年下半年公布多个临床试验的数据。尤其重要的是BRII-835和BRII-877的联合应用,以及加或不加PEG-IFNα的三联疗法给药48周治疗结束后的数据结果。对于那些目前未见明显疗效的高乙肝表面抗原基线患者来说,这可能带来新的希望。
乙型肝炎治疗功能性的突破性机会可能即将到来。通过20多年的持续研究,乙型肝炎疫苗的研发已经过半,哪家企业将成为首个突破终点线的,值得期待。

2025-04-06

2025-04-06

2025-04-06

2025-04-06

2025-04-06