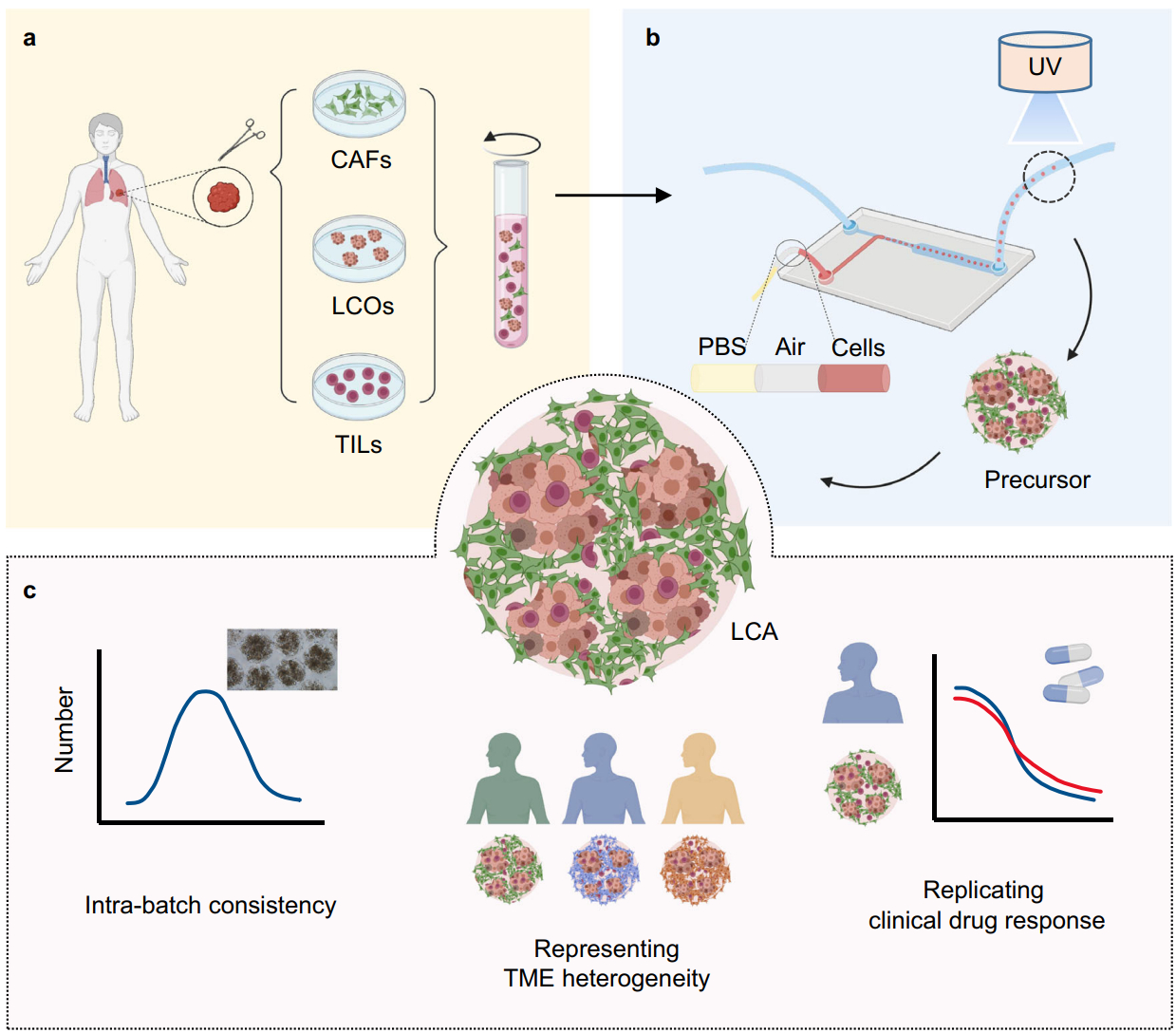
肿瘤模型对于肿瘤研究和治疗评估至关重要,同时也是抗肿瘤药物研发中的关键瓶颈。目前热门的肿瘤类器官模型存在着缺乏肿瘤微环境和批次内一致性低的问题。如何快速准确地建立含有异质性肿瘤微环境的个体化肿瘤模型,是当前亟待解决的重要问题,尤其在肿瘤研究和治疗领域。最近, 清华大学机械系的熊卓/张婷课题组、自动化系的古槿课题组与北京大学肿瘤医院等单位的研究人员共同组成了一个跨学科团队。团队创新性地提出了基于液滴微流控技术的个体化肺癌类组装体模型。该模型在批次内具有良好一致性,能够体外模拟个体肿瘤的异质性和微环境(包括免疫微环境),能够准确预测临床患者对药物的反应性。这为肿瘤的个性化治疗和药物的精准筛选提供了一个新的模型,具有重要的临床应用前景。研究小组已经成功研发了基于微量上样方法的液滴微流控技术,以及具有出色原代细胞生物相容性的水凝胶材料。这一技术解决了多种原代细胞共培养的关键问题。通过在水凝胶材料中包埋来源于肺癌患者的肺癌类器官(LCOs)和多种肿瘤微环境细胞,再经过流体剪切、光固化成型和快速培养,形成了类组装体模型(LCAs)。这一技术可以精确地对临床穿刺样本中微量细胞进行上样控制,同时类组装体模型可以直接冻存和复苏。通过针对分子、细胞和组织水平的研究,我们全面证实了类组装体与体内肿瘤的相似性。在药物筛选和临床药物反应预测实验中,我们验证了类组装体可作为药物精准筛选和个性化诊疗的模型。在《自然·通讯》杂志上发表了关于“具有不同肿瘤微环境的病人特异性肺癌集合体模型”的研究成果。张艳梅,北京市科学技术研究院副研究员,是清华大学机械系的前博士后;胡启帆,清华大学自动化系2020级博士生;裴宇权,北京大学肿瘤医院副主任医师,三人合作撰写的论文中,他们是第一作者。论文的通讯作者是清华大学机械系教授熊卓以及自动化系副教授古槿。这项研究涉及清华大学机械系和自动化系、北京市科学技术研究院、北京大学肿瘤医院、解放军总医院以及中国医学科学院肿瘤医院的研究人员。资助来源包括清华大学-丰田联合研究基金以及国家自然科学基金青年基金。