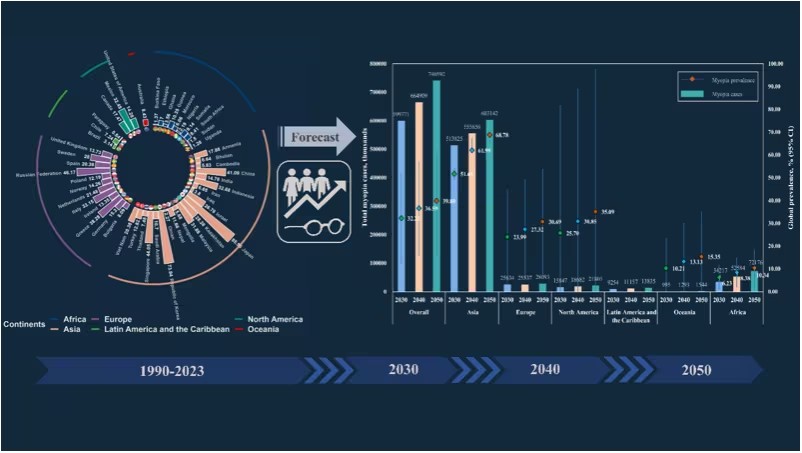
近日,中山大学公共卫生学院的陈亚军教授团队发布了一项重要研究,揭示了全球儿童青少年近视的严重性。研究显示,目前全球约每三名儿童青少年中就有一人患有近视,预计到2050年,近视患病人数将超过7.4亿。这项研究整合了1990年至2023年间来自50多个国家的276项研究数据,涵盖了540多万名儿童青少年,使用时间序列模型精确预测未来30年的近视患病率变化。相关成果以“Global
Prevalence, Trend and Projection of Myopia in Children and Adolescents from 1990
to 2050: A Comprehensive Systematic Review and
Meta-analysis”为题,发表在眼科领域权威期刊《英国眼科学杂志》。 近视问题已成为全球公共卫生的重要挑战,尤其在儿童青少年群体中,其患病率呈快速上升趋势。研究团队回顾了截至2023年6月的45,470篇相关研究与政府报告,通过严格的筛选标准,最终纳入了276项覆盖亚洲、欧洲、非洲、大洋洲、北美和拉丁美洲等50个国家的研究,涉及541万多名儿童青少年及近196万近视病例。研究通过随机效应模型估计全球儿童青少年近视的总体流行率和时间趋势,并采用自回归积分滑动平均模型预测2050年近视流行率。 研究结果显示,全球儿童青少年近视患病率为30.5%,并在过去30年间显著增加,从1990年的约24.3%增至2023年的30.5%。具体来看,1990至2000年间,近视患病率为24.3%;2001至2010年为25.3%;2011至2019年增至29.7%;而2020至2023年则显著攀升,青少年近视率高达54%。 经济发展水平显著影响近视患病率,发展中国家的近视患病率(31.9%)明显高于发达国家(23.8%)。在不同地区中,亚洲地区的近视患病率最高,达到35.2%;而拉丁美洲和加勒比地区最低,仅为3.8%。在本研究纳入的国家中,日本的儿童青少年近视患病率最高,达到86.0%,其次为韩国(73.9%)、俄罗斯(46.2%)和新加坡(44.1%);中国的近视患病率为41.1%,排在第五位。 年龄、性别和地区对近视患病率的影响也十分明显。整体而言,青少年的近视患病率高于儿童,且从1990年到2023年,儿童的近视患病率绝对增长率约为青少年的两倍。性别方面,女孩的近视患病率(33.6%)略高于男孩(30.5%),特别是青春期女孩的近视患病率达到48.8%。在城乡差异上,城市地区的儿童青少年近视患病率高于农村地区,城市女孩的近视患病率(32.0%)也高于男孩(29.4%)。 对中国儿童青少年近视的单独分析显示,研究共涉及1,891,986名中国儿童青少年,其中4,294,116名患有近视。整体而言,1990年至2023年,中国儿童青少年的近视总患病率为41.1%。不同地区的近视患病率差异明显,东部地区最高,为46.3%;西部和中部地区分别为37.8%和37.1%;而特别行政区(如香港和台湾)为31.3%,东北部地区为28.0%。性别差异方面,女孩的近视患病率(43.7%)高于男孩(39.7%),尤其广西的女孩近视患病率高达72.9%。 根据未来预测,全球儿童青少年的近视患病率预计将在2030年达到32.2%,影响近6亿儿童青少年;到2040年,近视患病率将上升至36.6%,影响超过6.6亿儿童青少年;而2050年,预计将继续上升至39.8%,影响超过7.4亿儿童青少年。相较于男孩,女孩的近视患病率预计更高,2050年将达到42.0%;与6-12岁儿童相比,13-19岁青少年的近视患病率可能更高,预计达到52.4%。发展中国家和不发达国家的儿童青少年近视患病率预计将达到40.8%,而亚洲地区将是近视患病率最高的区域,2050年预计达到68.8%。 综上所述,该研究为全球儿童青少年视力健康现状提供了全面的证据,建议儿童和青少年应增加户外活动,减少屏幕时间。考虑到社会、经济和文化背景的差异,公共卫生决策者应更加重视区域化的近视预防策略,以应对日益严峻的视力健康挑战。研究的共同第一作者包括中山大学公共卫生学院的博士生梁景宏、硕士生普迎琦和陈佳琦,陈亚军教授为论文的唯一通讯作者。该研究得到了国家自然科学项目和广东省自然科学基金项目的支持。